「イントロン型マイクロRNAとその宿主遺伝子の関連性の解明」 —最新ゲノム編集技術が新たな結論を導く—
2018年04月27日
明治大学
「イントロン型マイクロRNAとその宿主遺伝子の関連性の解明」
—最新ゲノム編集技術が新たな結論を導く—
—最新ゲノム編集技術が新たな結論を導く—
国立大学法人 東京医科歯科大学
国立研究開発法人 日本医療研究開発機構
学校法人 明治大学
国立研究開発法人 日本医療研究開発機構
学校法人 明治大学
ポイント
- 頭蓋骨の発達に関連のある遺伝子は複数知られていますが、イントロン型マイクロRNA(注)であるmiR-140が頭蓋骨発達異常の原因であることが確認されました。
- これまで、miR-140の宿主遺伝子であるWWP2も、頭蓋骨の発達に関連があると報告されていましたが、ゲノム編集技術CRISPR/Cas9法によって、これまで困難であった、宿主遺伝子とイントロン型マイクロRNAの個別及び同時の遺伝子欠損の作成が可能となり、頭蓋骨の発達との関連性を明らかにすることができました。
- 遺伝子改変マウスの作成において、ゲノム編集技術を用いることでより精度の高い知見を得ることができる可能性があり、今後の遺伝子改変マウスを用いた多くの実験に影響を与えることが期待されます。
※本研究開発領域は、平成27年4月の日本医療研究開発機構の発足に伴い、国立研究開発法人科学技術振興機構(JST)より移管されたものです。
研究の背景
図1 ジーントラップ法とCRISPR/Cas9法の違い
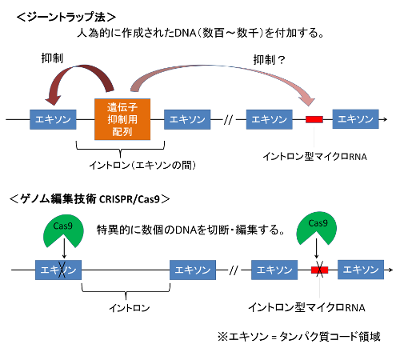
ジーントラップ法は、遺伝子の働きを抑える配列をゲノムに挿入する。一方、CRISPR/Cas9法は、Cas9というたんぱく質に特異的にDNAを認識させることによって、遺伝子の切断・編集が行われる。
図2 ジーントラップ法で作成されたWWP2欠損マウス(WWP2GT/GT)の頭蓋骨のマイクロCT像(下記論文情報より)
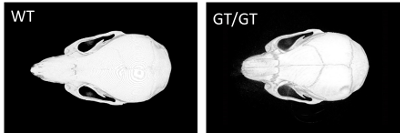
ジーントラップ法で作成されたWWP2欠損マウス(WWP2GT/GT)では、野生型(WT)と比較し、頭蓋骨短縮などの変化が認められる。
図3 miR-140欠損マウス(miR-140-/-)の頭蓋骨の骨格標本(参考文献2より)
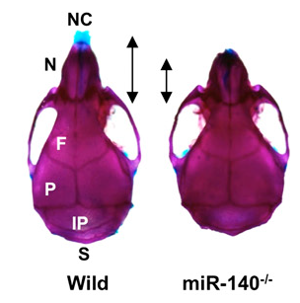
miR-140欠損マウス(miR-140-/-)では、野生型(Wild)と比較し、頭蓋骨短縮などの変化が認められる。
研究成果の概要
これらの結果は、遺伝子改変マウスを用いた研究を行う上で、類似した現象が生じる可能性を示していますので、炎症の慢性化機構やメカノバイオロジー機構に関する研究を進めていく上で、今後も留意すべきと考えられます。
図4 CRISPR/Cas9法で作成されたマウス3種類(WWP2KO, miR-140KO, miR-140/WWP2 double KO)のマイクロCT像(下記論文情報より)
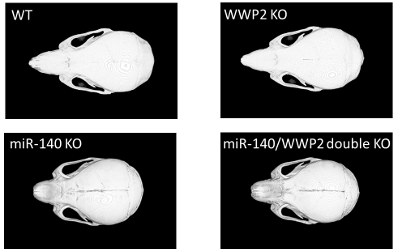
WWP2欠損マウス(WWP2KO)では、野生型(WT)と比べて、頭蓋骨短縮は認められないが、miR-140欠損マウス(miR-140KO)及びmiR-140/WWP2両欠損マウスでは図3の場合と同程度の頭蓋骨短縮を認められる。
研究成果の意義
(注) マイクロRNAには、固有のプロモーターを有し遺伝子間に存在するインタ—ジェニック型マイクロRNAと、イントロンにコードされ、宿主遺伝子とともに転写されるイントロン型マイクロRNAが存在します。イントロンとは、タンパク質コード領域の間の領域を示しています。
参考文献
2. Miyaki, S. et al. MicroRNA-140 plays dual roles in both cartilage development and homeostasis. Genes Dev 24, 1173–1185 (2010).
3. Inui M, et al. Rapid generation of mouse models with defined point mutations by the CRISPR/Cas9 system. Scientific Reports 4, 5396 (2014).
論文情報
論文タイトル:Dissecting the roles of miR-140 and its host gene.




- お問い合わせ先
-
研究に関すること
東京医科歯科大学大学院医歯学総合研究科
システム発生・再生医学分野 浅原弘嗣(アサハラ ヒロシ)
TEL:03-5803- 5015 FAX:03-5803- 5810Email:asahara.syst@tmd.ac.jp
-
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
〒113-8510 東京都文京区湯島1-5-45
TEL:03-5803-5833 FAX:03-5803-0272
E-mail:kouhou.adm@tmd.ac.jp
明治大学 経営企画部広報課
〒101-8301 東京都千代田区神田駿河台1-1
TEL:03-3296-4330 FAX:03-3296-4087
E-mail:koho@mics.meiji.ac.jp
-
AMEDに関すること
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課
TEL: 03-6870-2224 FAX: 03-6870-2246Email:kenkyuk-ask@amed.go.jp


